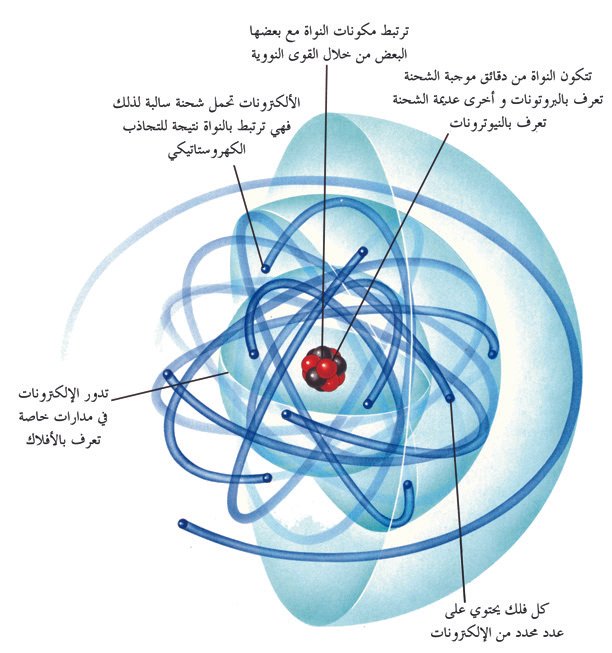
التركيب الذري Atomic structure
Posted in :
التركيب الذري Atomic structure :
(للصور و الأشكال التوضيحية يرجى تحميل ملف pdf المرفق )
For figures please download the pdf file
معلومات حول التركيب الذري Atomic structure
- بسبب معرفتنا الحديثة بالتركيب الذري ، تم تحقيق الكثير من الإنجازات في علم الكيمياء.
- طبقا للنظرية الذرية الحديثة فإن الذرة تتكون من نـواة موجبة الشحنة و من إلكترونـات سالبة الشحنة تدور في أفلاك حول النـواة.
- تحتوي النـواة على نوعين من الجسيمات و هما: البروتونات و النيوترونات . يحمل البروتون شحنة موجبة مقدارها +1، أما النيوترون فهو متعادل.
- إن كتلة الإلكتـرون ضئيلة جدا ، فتتركز كتلة الذرة كلها تقريبا في النـواة ، حيث يتساوى كل من كتلتي البروتون والنيوترون تقريبا.
- ذرة الهيدروجين هي أبسط الذرات و تتكون من بروتون واحد و إلكـترون يدور حول النـواة.
- العدد الذري يساوي عدد البروتونات الموجودة في نـواة الذرة.
- يساوي العدد الكتلي مجموع عددي البروتونات والنيوترونات في نـواة الذرة.
- العدد الكتلي لنظائر العنصر الواحد مختلفة ، أما أعددها الذرية فإنها متساوية.
- للهيدروجين ثلاثة نظائر ، منها نظيرين تحتوي نـواة كل منها على نيوترون (ديتريوم) أو نيوترونين (تريتيوم)
- يُعرف النظير بوضع عدده الكتلي أعلى يسار رمزه الكيميائي ، و يكتب العدد الذري أسفل يسار الرمز .
- تتكون أغلب العناصر من أكثر من نظير.
- تتحدّد الخواص الكيميائية للذرة بترتيب الإلكتـرونات فيها، و في الذرة المتعادلة يتساوى عدد الإلكتـرونات مع عدد البروتونات .
- طبقا للنظرية الذرية الحديثة ، لا يمكن تحديد مسارات الإلكتـرونات بكل دقة.
- يتحرك كل إلكتـرون في فلك معين و ذلك ضمن سحابة إلكتـرونية .
- يكون احتمال وجود الإلكتـرون كبيرا حيثما كانت كثافة السحابة الإلكتـرونية عالية و يكون هذا الاحتمال صغيرا حيثما كانت السحابة منخفضة .
- للأفلاك الإلكتـرونية أشكال مختلفة ، فمثلا للفلك s شكل كروي ، كما أنه يزداد حجمها ويزداد بعدها عن النـواة بزيادة عدد الكم الرئيسي .
- للفلك p ثلاثة أنواع مختلفة ، لها نفس الشكل و لكنها تختلف في الاتجاه .
- أفلاك d لها خمسة أشكال مختلفة .
- يدور الإلكتـرون حول نفسه أثناء سيره في فلكه ، ويكون دورانه إما في إتجاه عقارب الساعة أو في إتجاه عكس عقارب الساعة .
- يمكن أن يتسع الفلك لإلكتـرونين متزاوجين على الأكثر ، أي لإكترونين متضادي الدوران .
- تزداد طاقة الفلك بزيـــادة عدد الكـم الرئيسي . فمثلا 2s أعلى طاقة من 1s . كما أن طاقة الأفلاك المختلفة التي لها نفس عدد الكم الرئيسي مختلفـة في طاقتها ، فمثلا الفلك 2p أعلى طاقة من الفلك 2s . فالإلكتـرونــات تشغــل الأفلاك الأقل طاقة أولا ثم الأعلى طاقة .
- تملأ إلكتـرونات الذرة أفلاكها بترتيب تصاعدي للطاقة ، حيث يبدأ بالفلك 1s ثم 2s ثم 2p و هكذا .
يرجى تحميل ملف pdf
التركيب الذري Atomic Structure Akram Amir ElAli
بوسترات (لوحات) كيميائية بدقة عالية (أكثر من 25 لوحة) من تصميم الأستاذ أكرم أمير العلي
تطبيقات كيميائية من تصميم الأستاذ أكرم امير العلي متوفر للجوالات التي تعمل بنظام أندرويد android على سوق جوجل بلاي google play
1 – تطبيق ملصقات الجدول الدوري باللغة العربية : بطاقات تحتوي على معلومات شاملة و مختصرة في نفس الوقت كل عنصر على حدة (اللغة العربية).
https://play.google.com/store/apps/details?id=com.akramir2
2 – تطبيق ملصقات كيميائية: ملصقات بتصميم جميل جدا للكواشف و الأدلة و الزجاجيات المستخدمة في المختبر و كذلك ملصقات و بطاقات لخزانات حفظ المواد و الأدوات الزجاجية .
https://play.google.com/store/apps/details?id=com.akramir
3 – إذا كنت تواجه صعوبة في تحضير المحاليل الكيميائية الأكثر شيوعا في مختبرات الكيمياء و الاحياء، فهذا التطبيق سوف يساعدك كثيرا في تحضير المحاليل :