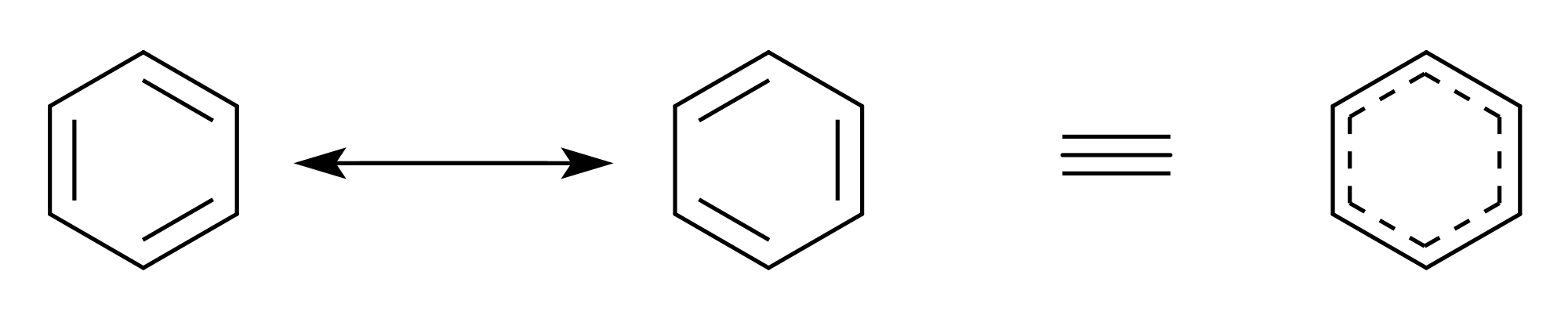
عدم التموضع ( اللاموضعية) للإلكترون Electron Delocalization
Posted in :
و يعرف أيضا بعدم التمركز أو اللاتمركز (لا متمركز) حيث في بعض المركبات العضوية لا يمكن اعتبار إلكترونات التكافؤ انها مرتبطة بالتحديد برابطة معينة بين ذرتين و لكن تكون ( منتشرة ) بين عدد من الذرات في الجزيء . مثل هذه الإلكترونات تعرف باسم الإلكترونات اللاموضعية . تحدث اللاتموضع عندما يحتوي المركب على روابط ثنائية او ثلاثية بديلة ( مرافقة ) ، و تكون الإلكترونات اللاموضعية هي تلك الموجودة في مدارات باي ، و في هذه الحالة يكون المركب اكثر استقرارا من تلك الحالة التي تكون فيها الالكترونات متموضعة و هذا يتجلى في حالة البنزين و بعض المركبات العطرية . مثال آخر على هذا الموضوع يظهر في أيونات الحموض الحموض الكربوكسيلية التي تحتوي على مجموعة الكربوكسيلات −COO− . في حالة الترابط البسيط فإن هذه المجموعة لديها ذرة كربون مرتبطة مع ذرة اكسجين برابطة ثنائية ( C=O ) و مع الأخرى برابطـــة أحادية ( −C−O ) . و في الحقيقة كلا الرابطتين بين الكربون و الأكسجين متماثلة بسبب تنقل الإلكترونات الزائدة التي على الاكسجين −O و التي في رابطة باي في C=O بين الذرات الثلاثة .