كلوريد السلفوريل Sulfuryl chloride
Posted in :
و يعرف أيضا باسم ثنائي أكسيد ثنائي كلوريد الكبريت Sulfur Dichloride Dioxide و هو سائل غير عضوي عديم اللون ذو رائحة نفاذة جدا و حتى ابخرته ممكن أن تسبب تلفا في جلد الإنسان و في الاغشية المخاطية . يتحول 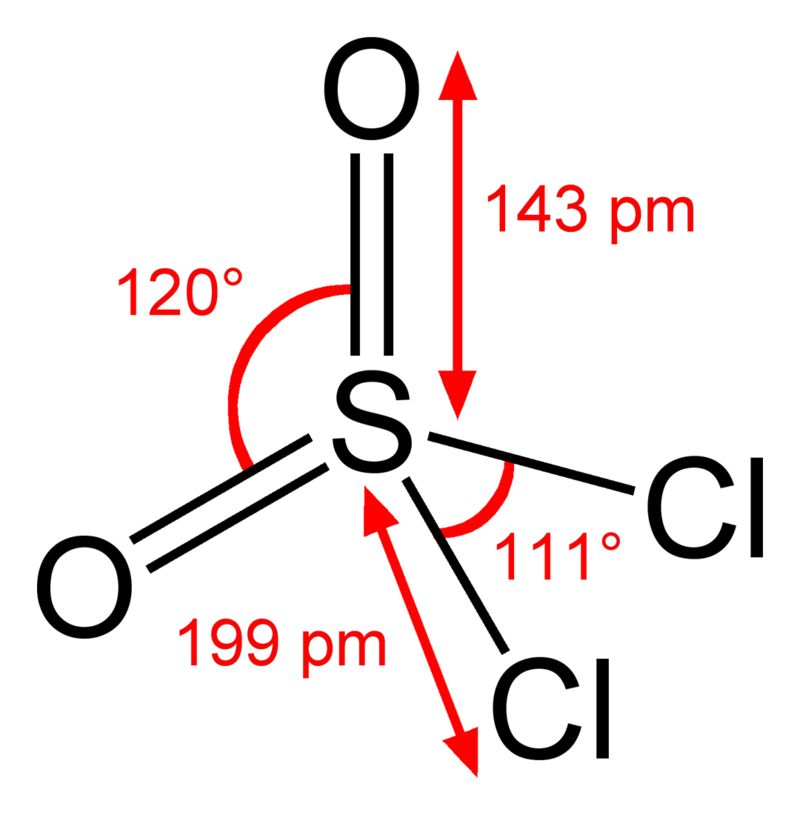
يتم تحضير كلوريد السلفوريل بواسطة تفاعل ثاني أكسيد الكبريت والكلور في وجود محفز ، مثل الكربون المنشط.
SO2 + Cl2 → SO2Cl2
يمكن تنقية المنتج الخام بالتقطير التجزيئي. من غير المألوف تحضير كلوريد السلفوريل في المختبر لأنه متوفر تجاريًا. كما يمكن أيضًا اعتبار كلوريد السلفوريل مشتقًا من حمض الكبريتيك.
تم تحضير كلوريد السولفوريل لأول مرة في عام 1838 من قبل الكيميائي الفرنسي هنري فيكتور رينو.
، و هو يستخدم كعامل كلورة و كمصدر لثاني أكسيد ثاني فلوريد الكبريت SO2F2 . و غالبا ما يستخدم كلوريد السلفوريل كمصدر للكلور. نظرًا لأنه سائل صالح للاستعمال ، فإنه يعتبر أكثر ملاءمة من الكلورللقياس والتخزين والاستغناء. يستخدم كلوريد السلفوريل على نطاق واسع ككاشف في تحويل C−H إلى C−Cl المجاور للبدائل المنشطة مثل الكربونيلات carbonyls و السلفوكسيدات sulfoxides. كما أنه يكلور الألكانات ، الألكينات ، الألكاينات ، العطريات ، الإثيرات (مثل رباعي هيدروفوران) والإيبوكسيدات. كما يمكن استخدامه أيضًا لتحويل الثيول أو ثاني كبريتيد إلى كلوريد السلفينيل المقابل ، على الرغم من أن كلوريد السلفوريل ينتج عن الثيول في بعض الحالات. [4] كما يعمل كلوريد السلفوريل يمكن أيضا تحويل الكحوليات إلى كلوريد ألكيل. في الصناعة ، و يستخدم كلوريد السلفوريل في إنتاج المبيدات الحشرية.و يمكن أيضًا استخدام كلوريد السلفوريل لعلاج الصوف لمنع الانكماش.