حمض الإيزوسيانيك isocyanic Acid
Posted in :
حمض غير مستقر قابل للانفجار صيغته الكيميائية HOCN ، و أيضا 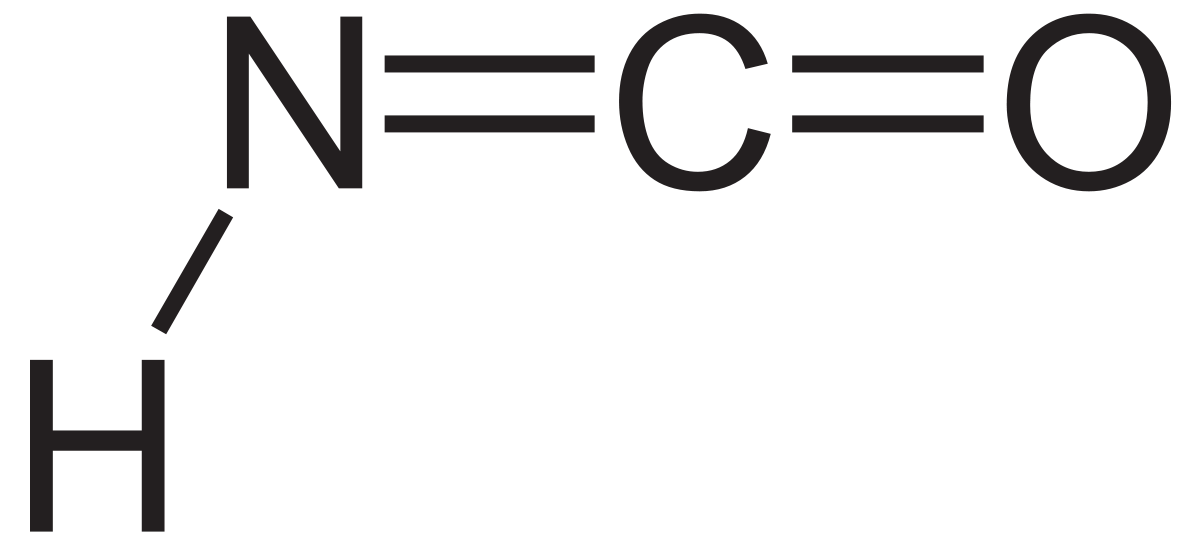
يمكن صنع حمض الإيزوسيانيك بواسطة برتنة أنيون السيانات ، من املاح مثل سيانات البوتاسيوم ، إما عن طريق كلوريد الهيدروجين الغازي أو من خلال حموض مثل حمض الأوكساليك.
H+ + NCO– → HNCO
و يمكن تحضير HNCO عن طريق التحلل الحراري العالي لحمض السيانوريك
C3H3N3O3 → 3 HNCO
يتحلل حمض الإيزوسيانيك إلى ثاني أكسيد الكربون والأمونيا:
HNCO + H2O → CO2 + NH3
في التركيزات العالية بما فيه الكفاية ، يتأكسد حمض الإيزوسيانيك ناتجا عن ذلك حمض السيانوريك والسياميلايد (مبلمر). عادة ما يتم فصل هذه الأنواع بسهولة عن منتجات تفاعل الطور السائل أو الغازي. و المحاليل المخففة من حمض الأيزوسيانيك مستقرة في المذيبات الخاملة ، مثل الأثير و الهيدروكربونات المكلورة.
يتفاعل حمض الإيزوسيانيك مع الأمينات ناتجا عن ذلك اليوريا (الكارباميد):
HNCO + RNH2 → RNHC(O)NH2.
و يسمى هذا التفاعل باسم الكاربميلة .
يوجد حمض الإيزوسيانيك أيضًا في أشكال مختلفة كالدخان مثلا ، بما في ذلك دخان السجائر . تم اكتشاف حمض الإيزوسيانيك باستخدام مقياس الطيف الكتلي و هو قابل للذوبان بسهولة في الماء ، مما يشكل خطرًا صحيًا على الرئتين.