خصائص عناصر السلسلة الانتقالية الأولى و التوزيع الإلكتروني وحالات التأكسد
Posted in :
خصائص عناصر السلسلة الانتقالية الأولى و التوزيع الإلكتروني وحالات التأكسد :
حسب تعريف الأيوباك IUPAC فإن الفلز الانتقالي هو”عنصر له ذرة تحتوي على غلاف فرعي d ممتلئ جزئيًا ، أو يمكن أن يؤدي إلى إنشاء الكاتيونات مع فلك فرعي d غير مكتمل “.
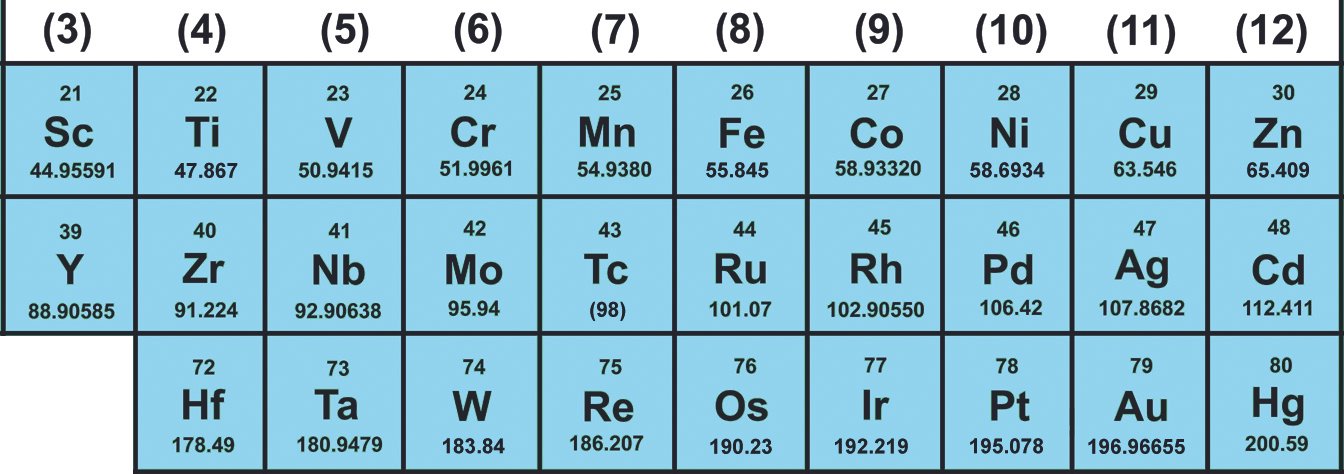
– و يصف العديد من العلماء “الفلز الانتقالي” بأنه أي عنصر يقع في القطاع d من الجدول الدوري والذي يتضمن مجموعات من 3 إلى 12 في الجدول الدوري و لكن فعليا ، تُعتبر سلسلة اللانثنيدات و الاكتنيدات و هي تنتمي إلى القطاع f من الجدول الدوري بأنها العناصر الانتقالية الداخلية”.
– قام كل من العالمين كونون و ويلكنسون بتوسيع تعريف الأيوباك IUPAC المختصر و المذكور أعلاه بتحديد العناصر التي يتم تعيينها ضمن العناصر الانتقالية . فبالإضافة إلى عناصر المجموعات من 4 إلى 11 ، فإنهما يضيفان السكانديوم والإيتريوم في المجموعة 3 والتي يكون فيها الفلك الفرعي d ممتليء جزئيا في الحالة الفيزيائية كما يتم تصنيف اللانثانوم والأكتينيوم في المجموعة 3 مع اللانثانيدات والأكتينيدات على التوالي.
و عليه يمكن تقسيم العناصر الانتقالية إلى صنفين و هما:
أ – العناصر الانتقالية الرئيسية (القطاع d ) و توجد في صلب الجدول الدوري و هي العناصر التي تُكوِّن أيونا واحدا على الأقل و تكون فيه أفلاك (مدارات) d ممتلئة إمتلاءً جزئيا ، أي أنها غير مكتملة الإلكترونات في الفلك d . و هي تقع في صلب الجدول الدوري و في الدورات الرابعة و الخامسة و السادسة و في المنطقة الفاصة بين القطاعين s على اليسار و القطاع p على اليمين.
ب – العناصر الانتقالية الداخلية (القطاع f) و توجد خارج أسفل الجدول الدوري و تتكون من سلسلة اللانثنيدات و سلسلة الاكتنيدات.
الخصائص العامة للعناصر الإنتقالية:
1 – جميعها معادن و بالتالي تتمتع بكل خواص المعادن من حيث جودة التوصيل للتيار الكهربائي و سهولة السحب و الطرق و تكوين سبائك مع الفلزات الأخرى و غيرها من الصفات.
2 – تشكل عددا كبيرا من الايونات الملونة و البارامغناطيسية و ذلك لوجود إلكترونات فردية. أما سبب تلون مركبات العناصر الإنتقالية فهذا يرجع إلى الإنتقالات الإلكترونية و هي نوعين :
أ – إنتقال d-d : حيث ينتقل الإلكترون بين فلكين (مدارين) من أفلاك d و يعطي هذا الانتقال ألوانا شاحبة (فاتحة).
ب – إنتقال إلكترون من فلك جزئي في الربيطة في مدار جزئي على ذرة الفلز أو العكس و يعطي هذا الانتقال ألوانا داكنة.
3 – لها القدرة على تكوين مركبات تناسقية (معقدة) مثل –Fe(CN)6]3] و سبب هذه الخاصية:
أ – ارتفاع شحنة أغلب الأيونات.
ب – وجود أفلاك (مدارات) d فارغة تسمح بدخول الأزواج الإلكترونية التي تتواجد على الرُبيطات (الليجاندات) .
4 – تعدد حالات الأكسدة و ذلك لأن الفرق في الطاقة الكلية بين الإلكترونات (d(n-1 و إلكترونات ns صغير مما يُمكن من استخدامها في التفاعلات الكيميائية.
5 – ذات خواص حفزية في التفاعلات الكيميائية و الصناعية و الحيوية ، فمثلا يستخدم أكسيد المنغنيز MnO2 في تفاعل تحلل فوق أكسيد الهيدروجين H2O2 .
6 – يتناقص نصف القطر الذري للعناصر من اليسار إلى اليمين خلال الدورة حتى قرب النهاية فإن الحجم يزداد فليلا.
7 – الاحجام الذرية للعناصر الانتقالية صغيرة لأن الزيادة في شحنة النواة تجذب الإلكتروناتإلى الداخل و بالتالي فإن كثافة العناصر الانتقاليى تكون كبيرة.
8 – بصفة عامة فإن درجات الانصهار و الغليان لأغلب العناصر الانتقالية عالية جدا. و تعتبر العناصر الخارصين Zn و الكادميوم Cd و الزئبق Hg مستثناه بسبب إمتلاء الفلك d بالإلكترونات.
9 – من ناحية انتشارها في الطبيعة نلاحظ أن عناصر الصف الأول زات الرقم الزوجي تكون اكثر انتشارا من العناصر التي تحتوي على أرقام ذرية احادية ، و الحالة الشاذة عنا هو المنجنيز. و عناصر الصف الثاني و الثالت أقل انتشارا من عناصر الصف الأول.
الصفات المغناطيسية لعناصر السلسلة الانتقالية الأولى :
تقسم المواد حسب طبيعة تفاعلاتها مع المجال المغناطيسي الخارجي حسب التركيب الإلكنروني للذرات أو الجزيئات أو الأيونات:
أ – مواد بارامغناطيسية : و هي المواد التني تنجذب نحو المجال المغناطيسي و يكون مقدار الحث المغناطيسي أكبر من أو يساوي 1 و المثال عليها أيونات فلزات القطاع d .
ب – المواد الدايامغناطيسية : و هي المواد التي لا تنجذب نحو المجال المغناطيسي و الحث المغناطيسي لها يساوي صفرا .
التوزيع الإلكتروني وحالات التأكسد لعناصر السلسلة الانتقالية الأولى
تزداد أعداد الأكسدة في السلسلة الانتقالية الأولى من السكانديوم Sc إلى الحد الأقصى في المنغنيز Mn ثم تنخفض مرة أخرى إلى الخارصين Zn باستثناء عناصر المجموعة IB ( أو المجموعة 11 و التي تشمل النحاس Cu و الفضة Ag و الذهب Au و البلاتين Pt) لأنه من السكانديوم Sc إلى المنجنيز Mn ، يزداد عدد الإلكترونات المزدوجة ومن المنجنيز Mn إلى الخارصين Zn تتوافر الإلكترونات المزدوجة .
توجد عناصر السلسلة الانتقالية الأولى في الدورة الرابعة بعد الكالسيوم 20Ca و الذي توزيعه الإلكتروني هو : Ar]4S2]، وبعد ذلك هناك ملء تدريجي للأفلاك الخمسة للمستوى الفرعي 3d بواسطة إلكترون واحد في كل فلك بالتسلسل حتى المنجنيز (3d5) ، و بعد المنجنيز يحدث غزدواج للإلكترونات في كل فلك حتى الخارصين (3d10) (قاعدة هوند).
بالنسبة للكروم والنحاس فإن التوزيع الإلكتروني للكروم Cr و النحاس Cu مختلف عن بقية العناصر الانتقالية. ففي حالة الكروم تكون الذرة مستقرة عندما يكون الغلافان الفرعيان 4s و 3d نصف ممتلئين ، أما في حالة النحاس فإن الغلاف الفرعي 4s يكون نصف ممتلئ و الغلاف الفرعي 3d ممتلئ بالإلكترونات.
24Cr : 1s2 2s2 2p6 3s2 3p6 4s2 3d4 خطأ
: 1s2 2s2 2p6 3s2 3p6 4s1 3d5 صح
29Cu : 1s2 2s2 2p6 3s2 3p6 4s2 3d9 خطأ
: 1s2 2s2 2p6 3s2 3p6 4s1 3d10 صح
| العنصر | العدد الذري | التوزيع الإلكتروني |
| ScandiumTitanium
Vanadium Chromium Manganese Iron Cobalt Nickel Copper Zinc |
21
22 23 24 25 26 27 28 29 30 |
[Ar]3d14s2 [Ar]3d24s2 [Ar]3d34s2 [Ar]3d54s1 [Ar]3d54s2 [Ar]3d64s2 [Ar]3d74s2 [Ar]3d84s2 [Ar]3d104s1 [Ar]3d104s2 |
و لا يمكن أن يتجاوز عدد التأكسد الأقصى لأي عنصر عن رقم مجموعته ، ويلاحظ الانحراف الوحيد عن تلك القاعدة في عناصر المجموعة IB ( أو المجموعة 11 و التي تشمل النحاس Cu و الفضة Ag و الذهب Au و البلاتين Pt)، ففي حالة التأكسد (عندما تفقد الذرة الإلكترونات) ، تفقد الذرة أولا الإلكترونات من 4S ثم يليه الإلكترونات من 3d و هذا يوفر حالات تأكسد مختلفة.
و تتميز العناصر الانتقالية بوجود العديد من حالات التأكسد ، نظرًا لأن المستوى الفرعي 3d غير ممتلئ تمامًا وبسبب أيضا قرب المستويات الفرعية (3d و4d) بالطاقة ، لذلك ، عندما تكتسب الذرة كمية تدريجية من الطاقة ، فإن الإلكترونين من المستوى الفرعي 4S يتم فقدها أولا ، ثم يتم فقد إلكترونات المستوى 3d تباعا، حيث أن الفرق في طاقات التأين صغير.
و تصبح الذرة أو الأيون مستقرة عندما يكون المستوى الفرعي d:
– فارغا (d0) كما في حالة +Sc3 و +Ti4 .
– نصف ممتليء (d5) كما في حالة +Mn2 و +Fe3.
– ممتليء بالكامل (d10) كما في حالة Zn + 2.
يتأكسد الحديد (II) بسهولة إلى الحديد (III) ، في حين لا يتأكسد المنغنيز (II) بسهولة إلى المنغنيز (III) ، فأيون الحديد (III) أكثر استقرارًا لأن المستوى الفرعي 3d يكون نصف ممتليء 3d5 ، وبالتالي فإن التفاعل يتجه نحو تكوين المركب الأكثر ثباتًا ، ولكن في حالة ذرة المنجنيز ، يكون التركيب الإلكتروني هو 25Mn: [Ar]3d5 ، 4S2 ، والمستوى الفرعي 3d نف ممتليء 3d5 في الأيون +Mn2 ، لذلك ، فهو أكثر ثباتًا من أيون (Mn (III ، لذلك لا يتأكسد أيون +Mn2 بسهولة إلى أيون +Mn3
+Fe2+ [18Ar] ، 3d6 (oxidation) → Fe3+ [18Ar] ، 3d5
Mn2+ ، 3d5 → Mn3+ ، 3d4
و من الصعب أكسدة أيون الحديد (III) إلى أيون IV ، في حين أنه من السهل أكسدة أيون التيتانيوم(III) إلى التيتانيوم IV لأن المستوى الفرعي (3d) يكون نصف ممتليء في +Fe3 وفارغا في +Ti4 مما يجعل العنصر أكثر استقرارا.
26Fe: [18Ar] 3d6 4S2 Fe3+ [18Ar]3d5 (الأكسدة) → Fe4+[18Ar]3d4
22Ti: [18Ar] 3d24S2 Ti3+ [18Ar] ، 3d1 (الأكسدة) → Ti4+[18Ar]3d0
تحتوي جميع عناصر السلسلة الانتقالية الأولى على حالة التأكسد (+2) لأنه بعد فقدان الإلكترونات من المستوى الفرعي (4s) في البداية (باستثناء السكانديوم) ، بينما في حالات التأكسد العليا ، تفقد إلكترونات (3d) تباعا.
تزداد حالات التأكسد من السكانديوم إلى المنجنيز الذي يحتوي على أعلى حالة أكسدة (+7) في المجموعة السابعة أو VIIB ، وبعد ذلك تنخفض حالات التأكسد تدريجياً لتصبح (+2) في الخارصين في المجموعة الثانية عشر أو IIB ، لذلك لا تتجاوز حالة التأكسد القصوى عن رقم مجموعتها باستثناء المجموعة الحادية عشر أو IB (مجموعة الفلزات النبيلة أو فلزات العملة و التي تحتوي على النحاس والفضة والذهب و البلاتين).
و تتميز العناصر الانتقالية الرئيسة بعدة حالات تأكسد، ويمكن تفسير ذلك على النحو التالي: عندما يتاكسد عنصر من العناصر الانتقالية من خلال فقدانه الإلكترونات من المستويات الفرعية 4s و 3d ,و التي هي متقاربة من حيث الطاقة ، فإن طاقات التأين للعنصر الإنتقالي تزداد تدريجيا.
الفلزات أو العناصر الممثلة مثل الصوديوم والمغنيسيوم والألمنيوم لها حالة تأكسد واحدة لأن طاقة التأين الثانية للصوديوم والثالثة للمغنيسيوم والرابعة للألومنيوم مرتفعة للغاية و بالتالي تكون هناك الحاجة إلى طاقة عالية لكسر مستوى طاقة بأكمله، لذلك ، من الصعب الحصول على +Na2 أو +Mg3 أو +Al4 أثناء التفاعل الكيميائي في الظروف الطبيعية.
فعنصر السكانيوم لا ينتج أيون +Sc4 بالطرق الكيميائية المعتادة ، ولا يحتوي السكانديوم إلا على حالة تأكسد واحدة (+Sc3) لأن الفرق بين طاقة التأين الثالثة و طاقة التأين الرابعة كبير للغاية بسبب كسر مستوى الطاقة .
و يعطي السكانديوم حالة تأكسد(+3) و ليس (+2) ، لأن الفرق بين طاقة التأين الثانية و طاقة التأين الثالثة صغير ، لذلك يفقد سكانديوم إلكترونين من المستوى الفرعي 4S ثم إلكترون واحد من مستوى فرعي 3d ليكون أكثر استقرارًا ، أي مشابها لاستقرار الأرجون .
و لا يشكل سكانديوم مركبات يكون للسكانديوم فيها حالة تأكسد(+2) لأنه عند إعطاء طاقة للسكانديوم ، فإنه يفقد ثلاثة إلكترونات ، وذلك لأن طاقة المستوى الثانوي (4S) قريبة من طاقة المستوى الفرعي (3d) ، لذلك ، تصبح الذرة أكثر ثباتًا والتكوين الإلكتروني للسكانديوم يصل إلى أقرب غاز خامل.
تعتبر فلزات العملة و هي للنحاس والفضة والذهب و البلاتين عناصر انتقالية لأنه في حالة التأكسد (+2) أو (+3) ، يحتوي المستوى الفرعي (d) على 9 أو 8 إلكترونات ، لذلك يشغلها الإلكترونات ، ولكن لا تشغلها بالكامل.
بوسترات (لوحات) كيميائية بدقة عالية (أكثر من 25 لوحة) من تصميم الأستاذ أكرم أمير العلي
تطبيقات كيميائية من تصميم الأستاذ أكرم امير العلي متوفر للجوالات التي تعمل بنظام أندرويد android على سوق جوجل بلاي google play
1 – تطبيق ملصقات الجدول الدوري باللغة العربية : بطاقات تحتوي على معلومات شاملة و مختصرة في نفس الوقت كل عنصر على حدة (اللغة العربية).
https://play.google.com/store/apps/details?id=com.akramir2
2 – تطبيق ملصقات كيميائية: ملصقات بتصميم جميل جدا للكواشف و الأدلة و الزجاجيات المستخدمة في المختبر و كذلك ملصقات و بطاقات لخزانات حفظ المواد و الأدوات الزجاجية .
https://play.google.com/store/apps/details?id=com.akramir
3 – إذا كنت تواجه صعوبة في تحضير المحاليل الكيميائية الأكثر شيوعا في مختبرات الكيمياء و الاحياء، فهذا التطبيق سوف يساعدك كثيرا في تحضير المحاليل :
6 thoughts on “خصائص عناصر السلسلة الانتقالية الأولى و التوزيع الإلكتروني وحالات التأكسد”
Leave a Reply Cancel reply
This site uses Akismet to reduce spam. Learn how your comment data is processed.










شكرا على بحثكم واتمنى منكم الاستمرار
وجعله الله فى ميزان حسناتكم
كل الشكر لكم لمروركم الكريم لموقعي
احسنتم 👍
شكرا جزيلا لمروركم الكريم
كان بحث مفيد جدا وجزيل الشكر والتقدير لناشره
شكرا لمروركم الكريم